5.2: Wo wird beim Auto CO2 ausgestoßen?
| Autoren: | |
| Publikation: | 9.3.2015 |
| Lernstufe: | 3 |
| Übersicht: | Ein Experiment macht deutlich, dass bei der Verbrennung CO2 entsteht. |
| Angestrebte Kenntnisse: |
|
| Wortschatz: | Verbrennung, fossile Brennstoffe, Kohlenstoffdioxid (CO2) |
| Dauer: | 1 Stunde |
| Material: |
Für jede Gruppe:
|
| Herkunft: | La main à la pâte, Paris |
Ausgangsfrage
Zu Beginn der Stunde fragt die Lehrerin: "Warum sagt man, dass Autos die Luft verpesten?". Die Schüler diskutieren eine Weile, bevor die Lehrerin weiterfragt: "Was passiert in einem Motor? Was verbraucht bzw. verbrennt ein Motor?". Nach und nach kommen die Schüler zu dem Schluss, dass bei der Verbrennung von Treibstoff Gase entstehen, und dass diese Gase Schadstoffe sein können.
Die Lehrerin erklärt, dass eins dieser Gase das Kohlenstoffdioxid (CO2) ist. Sie fragt die Schüler, ob sie dieses Gas kennen. Meistens kennen die Schüler CO2 im Zusammenhang mit der Atmung (CO2 ist ein Bestandteil der ausgeatmeten Luft). Sie wissen auch, dass Sprudel und andere kohlensäurehaltigen Getränke CO2 enthalten. Und auch über den Zusammenhang zwischen CO2 und der Erderwärmung haben sie in der Regel schon etwas gehört.
Oft verbinden die Schüler den Begriff Schadstoff mit schlechten Gerüchen. Die Lehrerin betont daher, dass CO2 geruchlos ist und etwaige Gerüche von anderen Verbrennungsprodukten herrühren. Eine andere wichtige Eigenschaft des CO2 ist seine Unsichtbarkeit. Der Hinweis auf die Atmung überzeugt: Wenn wir ausatmen, sieht man nichts (abgesehen von Wasserdampf bei kaltem Wetter).
Die Lehrerin fragt nun: "Wie lässt sich CO2 trotz seiner Geruchlosigkeit und Unsichtbarkeit nachweisen?". Im Allgemeinen werden die Schüler nicht darauf kommen, dass man dazu Kalkwasser [1] verwenden kann. Kalkwasser ändert in Kontakt mit CO2 sein Aussehen.
Gemeinsam denkt sich die Klasse ein Experiment aus, das zeigen soll, dass bei der Verbrennung CO2 entsteht. Wenn die Schüler nicht weiterkommen, zeigt ihnen die Lehrerin das zur Verfügung stehende Material.
Experiment
Die Schüler zeichnen den Aufbau des gemeinsam besprochenen Experiments und führen es anschließend durch. Zum Beispiel kann man eine Kerze in einem geschlossenen Glas brennen lassen. Zuvor wurde unten in das Glas etwas Kalkwasser gegossen. Am Ende der Verbrennung, wenn die Kerze erloschen ist, ist das Kalkwasser trüb. Das ist der Nachweis dafür, dass CO2 entstanden ist.

Abb. 1: Eine Kerze wird in ein Glas gestellt und angezündet. Wird der Deckel auf das Glas geschraubt, erlischt die Kerze nach kurzer Zeit. Das Kalkwasser ist trüb geworden [2].
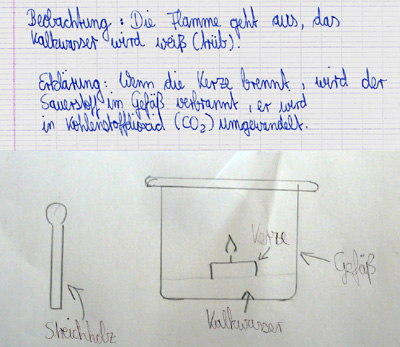
Abb. 2: Protokoll zum Experiment mit der Kerze im Glas [2]
Wissenschaftliche Anmerkungen
- Während der Verbrennung sieht man Rauch aufsteigen. Es handelt sich dabei nicht um das geruchlose und unsichtbare CO2, sondern um Kohlenstoff (feine Rußteilchen), der von der unvollständigen Verbrennung des Kerzenwachses herrührt (man kann den Ruß zum Beispiel nachweisen, indem man eine Glasplatte über die Flamme hält; die Glasplatte wird schwarz).
- Wenn die Verbrennung zu schnell endet (weil der Sauerstoff verbraucht ist) und für den Nachweis zu wenig CO2 entstanden ist, sollte man den Deckel des Glases nicht fest schließen. So kann die Verbrennung weitergehen, ohne dass zu viel CO2 entweicht (das CO2 neigt dazu, sich wegen seiner höheren Dichte am Boden des Glases zu sammeln).
Gemeinsame Erörterung
Der Versuch zeigt, dass durch die Verbrennung im Glas CO2 entstanden ist. Die Tatsache, dass das Kalkwasser trüb wird, beweist, dass in der Luft im Glas "etwas" ist, das in der Umgebungsluft nicht vorhanden ist.
Die Schüler können sich von der Reaktion des Kalkwassers überzeugen, indem sie ein entsprechendes Experiment mit ihrer Atemluft machen. Sie blasen durch einen Strohhalm Atemluft in das Kalkwasser und sehen, dass sich auch auf diese Weise eine Trübung einstellt.

Abb. 3: Ein Kind pustet seine Atemluft in die Kalkwasserlösung [2].
Zusammenfassung
Die Klasse erarbeitet eine gemeinsame Schlussfolgerung.
Beispiel: Bei der Verbrennung entsteht CO2 (Kohlenstoffdioxid).
Die Lehrerin fügt hinzu, dass CO2 als Schadstoff zu betrachten ist, weil es (in hoher Konzentration) gesundheitsschädlich ist, und vor allen Dingen weil der Ausstoß von CO2 die Hauptursache für den Klimawandel ist. Im Verbrennungsmotor entstehen allerdings noch weitere Schadstoffe: Gase und Teilchen, die wir im Laufe des Projekts noch untersuchen werden (siehe die Unterrichtseinheit "7.1: Auswirkungen des Verkehrs auf die Luftqualität").
Multimediale Erweiterung
Die Arbeitsweise des Verbrennungsmotors kann in der folgenden Animation untersucht werden.
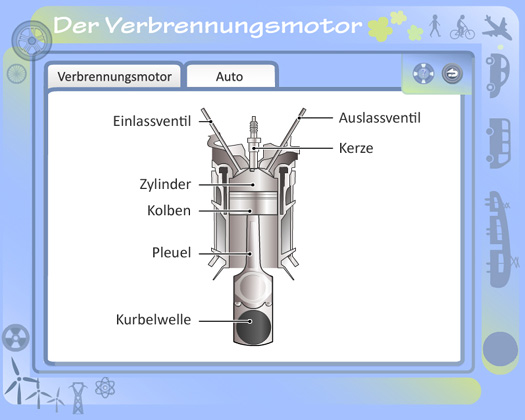
Abb. 4: Animation zur Funktionsweise des Verbrennungsmotors (auf Französisch)
In der Animation wird veranschaulicht, wie der Verbrennungsmotor funktioniert. Die Animation lässt sich auch ohne Französischkenntnisse verstehen. Es werden die vier Phasen (Takte) des Verbrennungsmotors dargestellt: 1. Ansaugen, 2. Verdichten, 3. Zünden und Ausdehnen, 4. Ausstoßen. Um die Geschwindigkeit zu erhöhen, kann man auf das Gaspedal "treten" Unter dem Reiter "Auto" (Voiture) kann man durch Drücken des Gaspedals sehen, wie der Motor schneller wird.
Mögliche Erweiterungen
Hier drei Möglichkeiten:
- Die Klasse kann der Frage nachgehen, wie man Autos herstellen kann, die weniger Schadstoffe ausstoßen. Dazu kann sie einfach mit dieser Unterrichtseinheit fortfahren und ein Solarauto entwerfen und bauen.
- Alternativ kann die Klasse näher auf die Auswirkungen des Autos auf die Umwelt eingehen. Das führt sie zu Teil 2, zu den Unterrichtseinheiten "7: Auswirkungen des Personen- und Güterverkehrs auf die Menschen und die Lebensqualität" und "8: Auswirkungen des Personen- und Güterverkehrs auf die Ökosysteme".
- Oder sie macht gleich mit Teil 3 weiter, um Alternativen zum Auto zu untersuchen, zum Beispiel "10 :Einrichtung eines 'laufenden Busses'" oder "11 :Verschiedene Verkehrsmittel – Multimodalität und Intermodalität" usw.
Fußnote
1:
Kalkwasser ist eine wässrige Kalciumhydroxid-Lösung, die man zum Nachweis von
CO2 verwenden kann. Man stellt Kalkwasser her, indem man Kalciumhydroxid
(Löschkalk) in Wasser gibt und die Lösung filtriert. In Kontakt mit CO2
wird das (vorher klare) Kalkwasser trüb.
Reaktion zum Nachweis von CO2 (Kalkwasser + Kohlenstoffdioxid wird zu
Kalziumkarbonat + Wasser):
Ca(OH)2 + CO2 → CaCO3 + H2O
2:
Abb. 1 und 2: 5. Klasse von Kévin Faix (Le Kremlin-Bicêtre)
Abb. 3: 5. Klasse von Cécile Perrin (Le Kremlin-Bicêtre)
Letzte Aktualisierung: 15.7.2025






